Découvrez quel élément a la valeur d'électronégativité la plus faible
 Share
Share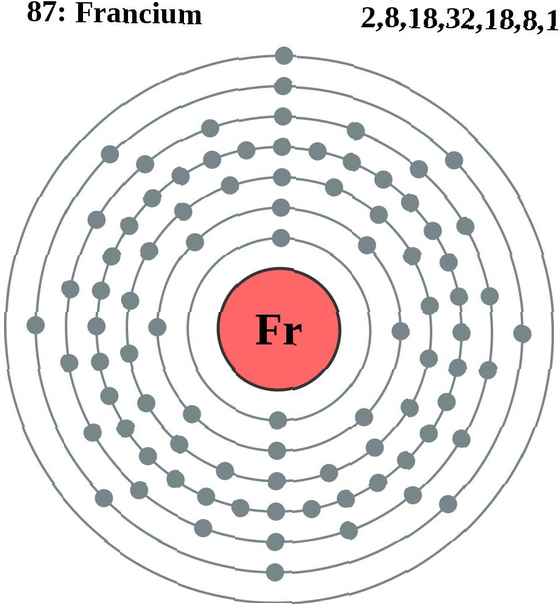
L'électronégativité est une mesure de la capacité d'un atome à attirer des électrons pour former une liaison chimique. Une électronégativité élevée reflète une capacité élevée à lier des électrons, tandis qu'une électronégativité faible indique une faible capacité à attirer des électrons. L'électronégativité augmente en se déplaçant du coin inférieur gauche du tableau périodique vers le coin supérieur droit.
L'élément ayant la valeur d'électronégativité la plus faible est le francium, qui a une électronégativité de 0,7. Cette valeur utilise l'échelle de Pauling pour mesurer l'électronégativité. L'échelle Allen attribue l'électronégativité la plus faible au césium, avec une valeur de 0,659. Le Francium a une électronégativité de 0,67 à cette échelle.
En savoir plus sur l'électronégativité
L'élément avec l'électronégativité la plus élevée est le fluor, qui a une électronégativité de 3,98 sur l'échelle d'électronégativité de Pauling et une valence de 1.
