Quels sont quelques exemples de composés covalents?
 Share
Share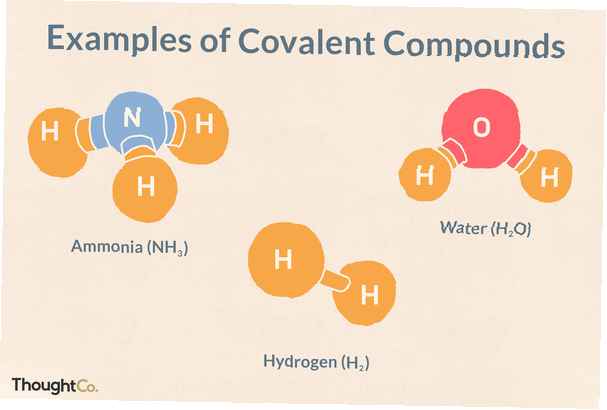
Ce sont des exemples de liaisons covalentes et de composés covalents. Les composés covalents sont également appelés composés moléculaires. Les composés organiques, tels que les glucides, les lipides, les protéines et les acides nucléiques, sont tous des exemples de composés moléculaires. Vous pouvez reconnaître ces composés car ils sont constitués de non-métaux liés les uns aux autres.
PCl3 - trichlorure de phosphore
CH3CH2OH - éthanol
O3 - ozone
H2 - hydrogène
H2O - eau
HCl - chlorure d'hydrogène
CH4 - méthane
NH3 - ammoniac
CO2 - gaz carbonique
Ainsi, par exemple, vous ne pas s'attendre à trouver des liaisons covalentes dans un métal ou un alliage, comme l'argent, l'acier ou le laiton. Vous trouveriez des liaisons ioniques plutôt que covalentes dans un sel, comme le chlorure de sodium.
Qu'est-ce qui détermine si une obligation covalente se forme?
Des liaisons covalentes se forment lorsque deux atomes non métalliques ont des valeurs d'électronégativité identiques ou similaires. Ainsi, si deux non-métaux identiques (par exemple, deux atomes d'hydrogène) se lient ensemble, ils formeront une liaison covalente pure. Lorsque deux non-métaux différents forment des liaisons (par exemple, l'hydrogène et l'oxygène), ils formeront une liaison covalente, mais les électrons passeront plus de temps plus près d'un type d'atome que l'autre, produisant une liaison covalente polaire.
