Quels sont les éléments du corps humain?
 Share
Share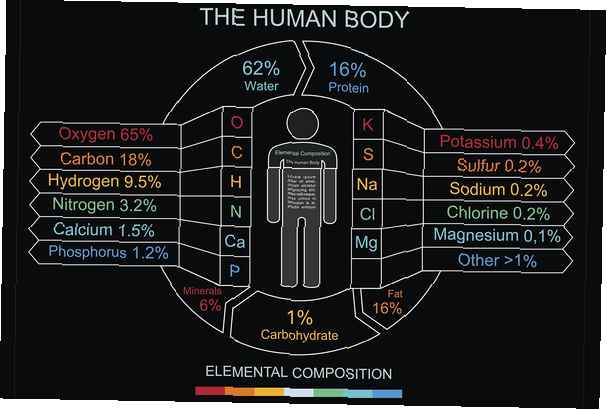
Il existe plusieurs façons de considérer la composition du corps humain, notamment les éléments, le type de molécule ou le type de cellules. La majeure partie du corps humain est constituée d'eau, H2O, avec des cellules constituées de 65 à 90% d'eau en poids. Par conséquent, il n'est pas surprenant que la majeure partie de la masse d'un corps humain soit de l'oxygène. Le carbone, l'unité de base des molécules organiques, vient en deuxième position. 99% de la masse du corps humain est composée de seulement six éléments: l'oxygène, le carbone, l'hydrogène, l'azote, le calcium et le phosphore.
- Oxygène (O) - 65% - L'oxygène et l'hydrogène forment de l'eau, qui est le principal solvant présent dans le corps et est utilisé pour réguler la température et la pression osmotique. L'oxygène se trouve dans de nombreux composés organiques clés.
- Carbone (C) - 18% - Le carbone possède quatre sites de liaison pour d'autres atomes, ce qui en fait l'atome clé de la chimie organique. Les chaînes de carbone sont utilisées pour fabriquer des glucides, des graisses, des acides nucléiques et des protéines. Rompre les liens avec le carbone est une source d'énergie.
- Hydrogène (H) - 10% - L'hydrogène se trouve dans l'eau et dans toutes les molécules organiques.
- Azote (N) - 3% - L'azote se trouve dans les protéines et dans les acides nucléiques qui composent le code génétique.
- Calcium (Ca) - 1,5% - Le calcium est le minéral le plus abondant dans le corps. Il est utilisé comme matériau structurel dans les os, mais il est essentiel pour la régulation des protéines et la contraction musculaire.
- Phosphore (P) - 1,0% - Le phosphore se trouve dans la molécule ATP, qui est le principal vecteur d'énergie dans les cellules. On le trouve également dans les os.
- Potassium (K) - 0,35% - Le potassium est un électrolyte important. Il est utilisé pour transmettre les impulsions nerveuses et la régulation du rythme cardiaque.
- Soufre (S) - 0,25% - Deux acides aminés comprennent le soufre. Les formes de soufre des liaisons aident à donner aux protéines la forme dont elles ont besoin pour remplir leurs fonctions.
- Sodium (Na) - 0,15% - Le sodium est un électrolyte important. Comme le potassium, il est utilisé pour la signalisation nerveuse. Le sodium est l'un des électrolytes qui aide à réguler la quantité d'eau dans le corps.
- Chlore (Cl) - 0,15% - Le chlore est un important ion chargé négativement (anion) utilisé pour maintenir l'équilibre des fluides.
- Magnésium (Mg) - 0,05% - Le magnésium est impliqué dans plus de 300 réactions métaboliques. Il est utilisé pour construire la structure des muscles et des os et est un cofacteur important dans les réactions enzymatiques.
- Le fer (Fe) - 0,006% - Le fer se trouve dans l'hémoglobine, la molécule responsable du transport de l'oxygène dans les globules rouges.
- Cuivre (Cu), Zinc (Zn), Sélénium (Se), Molybdène (Mo), Fluor (F), Iode (I), Manganèse (Mn), Cobalt (Co) - total moins de 0,70%
- Lithium (Li), Strontium (Sr), Aluminium (Al), Silicium (Si), Plomb (Pb), Vanadium (V), Arsenic (As), Brome (Br) - présent en traces
De nombreux autres éléments peuvent être trouvés en quantités extrêmement faibles. Par exemple, le corps humain contient souvent des traces de thorium, d'uranium, de samarium, de tungstène, de béryllium et de radium. Les oligo-éléments considérés comme essentiels chez l'homme comprennent le zinc, l'iode, éventuellement le silicium, probablement le bore, le sélénium, probablement le nickel, le chrome, le manganèse, le lithium, éventuellement l'arsenic, le molybdène, le cobalt et éventuellement le vanadium.
Tous les éléments du corps ne sont pas essentiels à la vie. Certains sont considérés comme des contaminants qui ne semblent pas nuire, mais ne remplissent aucune fonction connue. Les exemples incluent le césium et le titane. D'autres sont activement toxiques, notamment le mercure, le cadmium et les éléments radioactifs. L'arsenic est considéré comme toxique pour l'homme, mais remplit une fonction chez d'autres mammifères (chèvres, rats, hamsters) en quantités infimes. L'aluminium est intéressant car il est le troisième élément le plus courant dans la croûte terrestre, mais ne remplit aucune fonction connue dans les cellules vivantes. Alors que le fluor est utilisé par les plantes pour produire des toxines protectrices, il ne joue aucun rôle biologique essentiel chez l'homme.
Vous pouvez également souhaiter visualiser la composition élémentaire d'un corps humain moyen en masse.
Sources
- Chang, Raymond (2007). Chimie, 9e édition. McGraw-Hill. ISBN 0-07-110595-6.
- Emsley, John (2011). Blocs de construction de la nature: un guide de A à Z sur les éléments. OUP Oxford. p. 83. ISBN 978-0-19-960563-7.
- Frausto Da Silva, J. J. R; Williams, R. J. P (2001-08-16). La chimie biologique des éléments: la chimie inorganique de la vie. ISBN 9780198508489.
- H. A., V. W. Rodwell; P. A. Mayes, Examen de la chimie physiologique, 16e éd., Lange Medical Publications, Los Altos, Californie 1977.
- Zumdahl, Steven S. et Susan A. (2000). Chimie, 5e édition. Houghton Mifflin Company. p. 894. ISBN 0-395-98581-1.
